Anyon ve Katyon Nedir ?

Pow
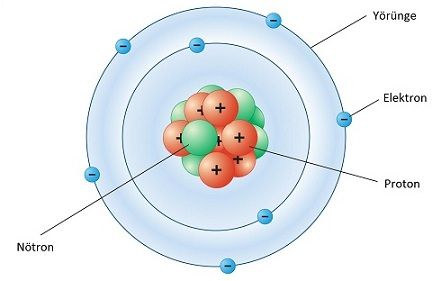
Nötr (Yüksüz) Atom Bir atom, merkezinde pozitif (+) elektrik yükü taşıyan bir çekirdek ile bu çekirdeğin çevresindeki belirli yörüngelerde (enerji düzeylerinde
Nötr (Yüksüz) Atom
Bir atom, merkezinde pozitif (+) elektrik yükü taşıyan bir çekirdek ile bu çekirdeğin çevresindeki belirli yörüngelerde (enerji düzeylerinde) dolanan ve negatif (-) elektrik yükü taşıyan elektronlardan oluşur. Normal şartlar altında, çekirdeğin taşıdığı artı elektrik yükü elektronların taşıdığı eksi elektrik yüküne eşittir ve bu iki yük birbirini dengeler. Böyle bir atom, elektriksel bakımdan dışarıya karşı nötr (yüksüz) bir durumdadır. Ayrıca nötr bir atomda artı elektrik yüklü protonların sayısı eksi elektrikli yüklü elektronların sayısına eşittir.
İyon
Nötr durumdaki bir atom, en dış yörüngesindeki elektronlarından bir veya bir kaçını kaybeder veya dışarıdan bir veya bir kaç elektron kazanırsa, elektrik yüklü hale gelerek iyon haline dönüşmüş olur. Elektron kazanarak veya kaybederek elektrik yüklü hale gelmiş olan atom veya atom gruplarına iyon denir. İyonlar, anyon ve katyon olmak üzere ikiye ayrılırlar.
Anyon ve Katyonlar
Anyon: Bir veya birkaç elektron kazanarak eksi elektrik yüklü hale gelen atom veya atom grubuna anyon denir. Anyonlar - yüklü iyonlardır. Örneğin Clˉ, Oˉ², Pˉ³, OHˉ, HCO₃ˉ, SO₄ˉ² iyonları birer anyondur.
Katyon: Bir veya birkaç elektron kaybederek artı elektrik yüklü hale gelen atom veya atom grubuna katyon denir. Katyonlar + yüklü iyonlardır. Örneğin Na⁺, Mg⁺², Al⁺³, NH₄⁺, H₃O⁺, NO₃⁺ iyonları birer katyondur.
Anot ve Katot
Bazen anyon-katyon, anot-katot, anyon-anot veya katyon-katotun ne olduğu birbirine karıştırılabilmektedir.
Moleküllerin artı ve eksi yüklü iyonlara ayrışmasına iyonlaşma denir. Örneğin sofra tuzu olarak da bilinen NaCl (sodyum klorür) suya bırakıldığında Na⁺ ve Clˉ iyonlarına ayrışarak çözünür. Çünkü su, sodyum ve klor iyonlarının arasına girerek aralarındaki çekim kuvvetini zayıflatıp birbirlerinden ayrılmasını sağlar.
NaCl (suda) → Na⁺ (suda) + Clˉ (suda) (NaCl'ün suda çözünmesi)
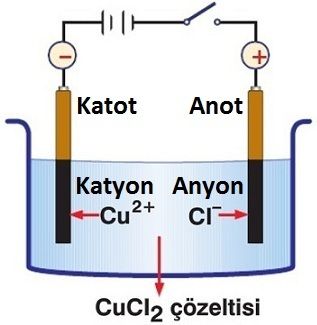
Bir elektrik pilinin eksi ve artı kutuplarına bağlı iki teli iyonlarına ayrışmış bir çözeltinin içerisine daldırırsak, her tel taşıdığı elektrik yüküne zıt yüklü iyonları kendine doğru çekerek çözelti içerisinde bir elektrik akımı oluşmasını sağlar. - yüklü iyonlar olan anyonları çeken anlamında, + yüklü kutba anot denir iken , + yüklü iyonlar olan katyonları çeken anlamında, - yüklü kutba ise katot denir.
Share Your Expertise, Earn Rewards!
Found this insightful? Imagine your knowledge generating income. Contribute your articles to bylge.com and connect with readers while unlocking your earning potential.