İzotop Atom

Pow
Bir elementin proton sayısı aynı nötron sayısı farklı olan atomlarına izotop denir. İzotop terimi Yunanca “aynı” anlamına gelen isos ve “yer” anlamına gelen to
Bir elementin proton sayısı aynı nötron sayısı farklı olan atomlarına izotop denir. İzotop terimi Yunanca “aynı” anlamına gelen isos ve “yer” anlamına gelen topos sözcüklerinin birleştirilmesinden türetilmiştir ve “aynı yerde bulunan” anlamına gelmektedir. Periyodik cetvelde elementler atom numarasına (proton sayısı) göre yerleştirilirler ve bir elementin bütün izotop atomları proton sayıları aynı olduğu için periyodik cetvelde aynı yerde bulunurlar.
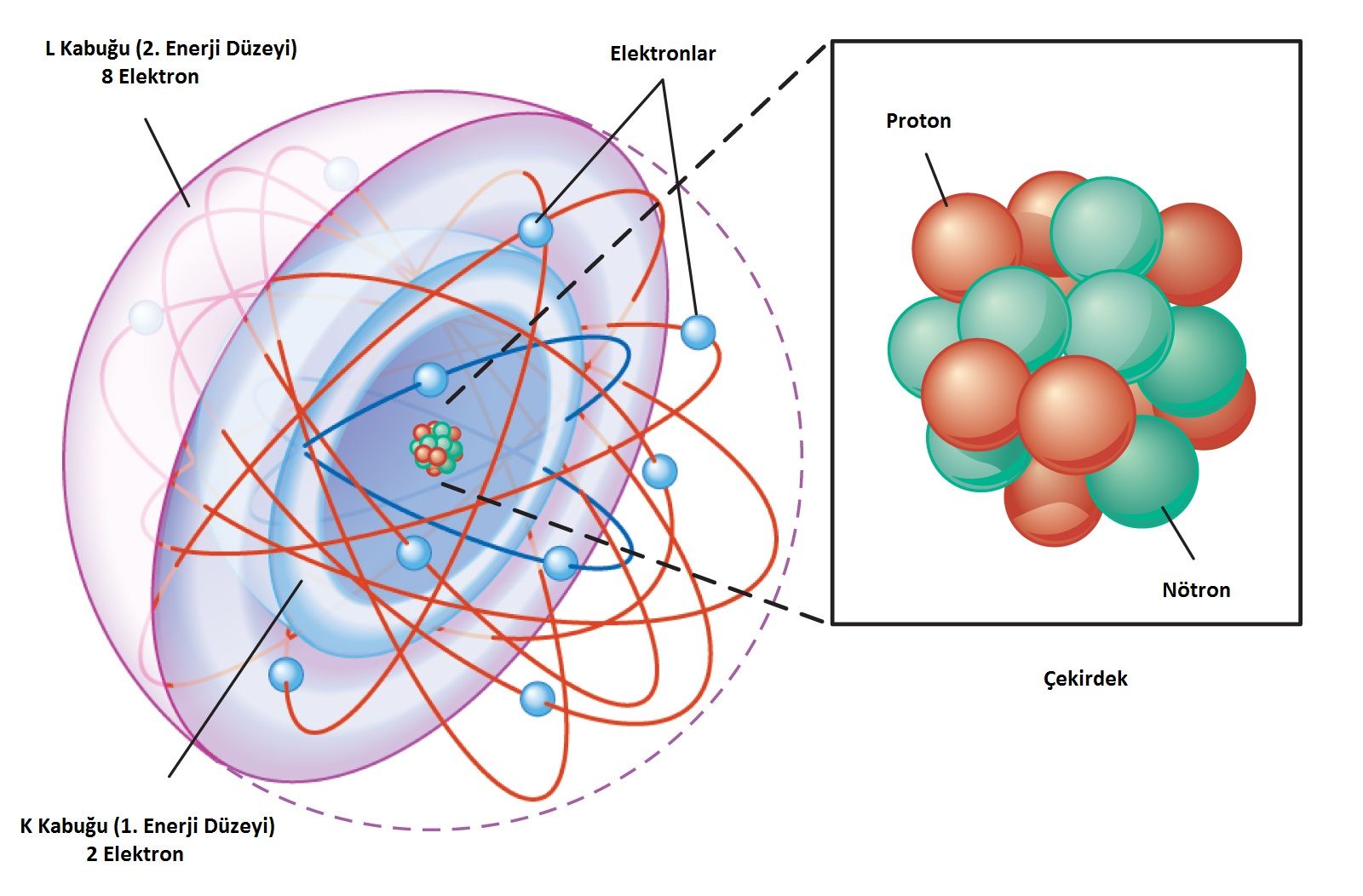
Doğadaki bütün elementler atom denilen çok küçük taneciklerden oluşmuşlardır. Bir atom, merkezinde çekirdek ve çekirdeğin etrafında belirli yörüngelerde (enerji düzeyleri) dolanan elektronlardan oluşur. Çekirdekte ise artı yüklü proton ve yüksüz nötron denilen tanecikler bulunur. Elektronlar ise eksi yüklüdürler. Bir atomun kütlesinin büyük bir kısmı (%99,9) çekirdekte yoğunlaşmıştır ve elektronların kütlesi protonların ve nötronların kütlesi yanında ihmal edilecek kadar küçüktür.
Her bir elementin bir diğerinden farklı fiziksel ve kimyasal özelliklere sahip olması ve birbirlerine hiç benzememesinin nedeni çekirdeklerindeki proton sayısından kaynaklanmaktadır. Örneğin platinin atom numarası 78 ve altının atom numarası 79’dur. Bu durum bir platin atomunun çekirdeğinde 78 ve bir altın atomunun çekirdeğinde 79 proton olduğu anlamına gelmektedir. İşte Bu iki elementin çekirdeklerindeki proton sayısının farklı olması altını altın yaparken platini de platin yapar. Atomlar için proton sayısı adeta bir kimlik veya parmak izi gibi ayırt edici bir özelliktir. Mesela nükleer fizikle uğraşan bilim adamları altın atomlarının çekirdeklerindeki bir protonu uzaklaştırarak altını platine dönüştürmeyi başardılar ama platin de en az altın kadar az bulunan ve değerli bir metal olduğu için çok pahalıya mal olan bu üretim yöntemi pek bir yarar sağlamadı.
1913 Yılında İngiliz bilim adamı Frederick Soddy nükleer fiziğe “izotop” kavramını kazandırarak çok büyük bir katkıda bulundu. O dönem deki birçok bilim adamı, yapmış oldukları pek çok sayıdaki radyoaktif bozunma deneyi sırasında ortaya çıkan ürünleri inceleyerek bunların aslında yeni birer element olduğunu düşündüler. Ancak Frederick Soddy, bu yeni ürünlerin aslında doğa da bulunduğunu bildiğimiz elementlerin yalnızca atom ağırlıkları (kütle numarası ) farklı değişik biçimleri olduğunu tespit etti ve asıl elementin bütün kimyasal özelliklerini taşıyan fakat ağırlıkları farklı olan bu atomlara izotop adını verdi. O dönem henüz daha nötronların varlığı bilinmediği için nötron sayıları farklı kelimesi yerine atom ağırlıkları farklı kelimesi kullanılmıştır ve nötronlar ancak 1932 yılında yine bir İngiliz olan Sir James Chadwick tarafından keşfedilebilmiştir.
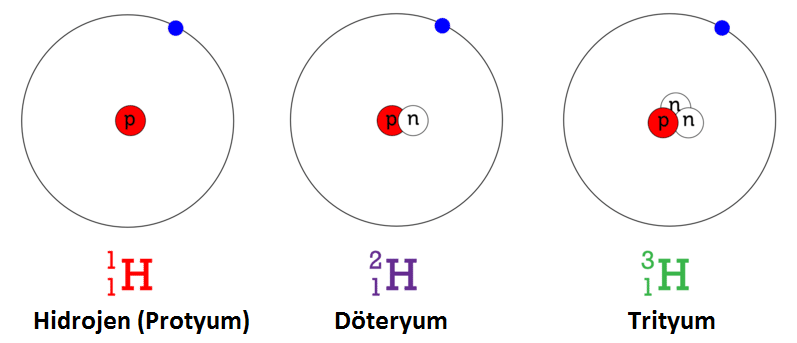
Yukarıdaki şekil de hidrojenin üç izotopunu görmektesiniz. Hidrojen dışındaki diğer bütün elementlerin izotopları kütle numaralarıyla adlandırılırken hidrojenin üç izotopundan her birine farklı özel bir isim verilmiştir. Örneğin sudaki hidrojenin %99,98’ini protyum, %0,02’sini döteryum ve elementin tek radyoaktif izotopu olan trityum ise çok küçük bir yüzdesini oluşturmaktadır. Hidrojenin bağıl atom kütlesi izotoplarının doğa da ki bulunma yüzdeleri hesaba katıldığında yaklaşık olarak 1.00797'dir.
Share Your Expertise, Earn Rewards!
Found this insightful? Imagine your knowledge generating income. Contribute your articles to bylge.com and connect with readers while unlocking your earning potential.